Aufgrund des gestiegenen Bewusstseins für Lebensmittelhygiene wurde die European Hygienic Engineering and Design Group (EHEDG) gegründet.
Dieser Artikel wird auf folgende Themen eingehen:
- Hygienische Designrichtlinien
- Testverfahren
- Testteil der Reinigungsverfahren
- Erkennung von Rückständen
- Reinigungsbewertung und -interpretation
Die Experten von Dinnissen Process Technology stehen Ihnen für all Ihre Fragen zur Verfügung:
Nehmen Sie Kontakt auf Juul Jenneskens 077 467 3555
Hygienische Gestaltungsrichtlinien
Die EHEDG hat hygienische Gestaltungsrichtlinien entwickelt, die durch Standardtestverfahren verifiziert werden können, die sich auf hygienisches Design beziehen. Dies umfasst Reinigbarkeit, Pasteurisierbarkeit, Serialisierbarkeit und aseptische Fähigkeiten.
Das Testverfahren ist ein grundlegender Screening-Test, um Bereiche mit schlechtem hygienischen Design zu identifizieren und solche, in denen Produkt- oder Mikroorganismen gegen die Wirkung des Reinigungsprozesses geschützt sind. Es kann auch verwendet werden, um Geräte hinsichtlich ihrer Reinigbarkeit an ihrem Platz zu vergleichen. Der Test ist nicht indikativ für die Leistung in industriellen Reinigungssituationen.
Der Reinigungsgrad basiert auf der Entfernung eines Bodens, der Bakterien enthält, und wird bewertet, indem das Wachstum der verbleibenden Bakterien nach der Reinigung untersucht wird. Die folgenden Begriffe werden hierfür verwendet:
- Reinigung: Das Entfernen von Schmutz, Lebensmittelresten, Abfällen, Fett oder anderen störenden Stoffen,
- Reinigbarkeit: Die Eignung von Geräten, um leicht von Schmutz befreit zu werden,
- Vergleichende Reinigbarkeit: Die Reinigbarkeit von Geräten im Vergleich zu einer Referenz,
- Reinigbarkeit vor Ort: Die Eignung, um ohne Demontage leicht gereinigt zu werden.

EHEDG
Testprocedure
Zuerst muss ein Testbereich gebildet werden. Dies geschieht, indem das zu testende Gerät mit einem Referenzrohr von 250 mm verbunden wird. Mit der bekannten inneren Oberflächenrauheit (durchschnittlich Ra = 0,5 - 0,7 Mikrometer oder äquivalent gemäß ISO 4287: 1977) und mit zwei kurzen Hilfsrohren an jedem Ende wird ein Testbereich gebildet.
Anschließend wird der Testbereich mit saurer Milch gefüllt und beide Enden werden verschlossen. Danach wird der Testbereich dreimal auf 5 bar Druck gebracht, unter Verwendung einer Abschlussplatte mit einer geeigneten Luftkupplung, für jeweils zwei Minuten. Es ist möglich, eine Inbetriebnahmesituation des Testbereichs zu simulieren, indem alle beweglichen Teile betätigt werden. Insgesamt müssen 10 Operationen innerhalb der 3 unter Druck stehenden Perioden durchgeführt werden.
Anschließend wird die saure Milch abgelassen und der Testbereich durch Spülen mit trockener gefilterter Luft getrocknet.
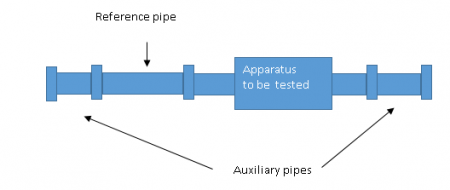
Testverfahren
Reinigungsverfahren des Testbereichs
Zur Reinigung wird der verschmutzte Testbereich in einer speziell dafür gebauten Testaufstellung montiert, ohne die Hilfsleitungen zu entfernen. Ein gerades Rohr mit einer Länge, die mindestens fünfmal so lang ist wie der Durchmesser des Referenzrohrs, muss vor und nach dem Testbereich eingeführt werden, um einen stabilisierten Fluss der Reinigungsflüssigkeit durch den Testbereich zu gewährleisten. Danach kann das folgende Reinigungsverfahren beginnen:
- Spülen mit kaltem Wasser (10-20°C) für eine Zeit, die der durchschnittlichen Verweilzeit (t) entspricht und mindestens 1 Minute beträgt,
- Zirkulieren einer 1%-igen (w/v) Waschmittelösung bei 63°C +/- 20°C für 10 Minuten (das Volumen der verwendeten Waschmittelösung muss mindestens 20-mal das Innenvolumen des Testobjekts betragen),
- Spülen mit kaltem Wasser (10-20°C) für eine Zeit, die der durchschnittlichen Verweilzeit (t) entspricht und mindestens 1 Minute beträgt.
Dabei gilt die durchschnittliche Verweilzeit (t) = Volumen des Testobjekts / Durchflussgeschwindigkeit.
Am Auslass der Geräte werden am Ende der Spülverfahren so genau wie möglich Wasserproben von beiden Spülvorgängen entnommen. Für jedes Petrischale werden zwei 5-ml-Proben mit MSHA gegossen. Während des Vorspülens werden 3-300 Sporen pro 10 ml zurückgewonnen. Nach der letzten Spülung sollte <1 Spore pro 10 ml wiederhergestellt werden. Weniger als 1 Spore pro 10 ml im Vorspülen oder das Vorhandensein von Sporen in der letzten Spülung kann auf ein unzureichendes Testverfahren hinweisen und zu falschen Ergebnissen führen.
Erkennung von Rückständen
Nach der Reinigung wird der Testbereich aus der Vorrichtung entfernt. Die Innenfläche des Referenzrohrs wird mit geschmolzenem MSHA bis zu einer Dicke von mindestens 5 mm bedeckt, einschließlich aller relevanten Oberflächen der Testgeräte. Nachdem das Agar vollständig erstarrt ist, wird das Referenzrohr für 24 Stunden fast vertikal in einen Inkubator bei 58°C gestellt. Es kann sein, dass Kondensation im Referenzrohr während der Inkubation Mikroorganismen und/oder saure mikrobielle Stoffwechselprodukte entlang des Referenzrohrs verbreitet. In diesem Fall wird eine falsche Ablesung der gelben Verfärbung erzielt.
Das Prinzip hinter dem Tap-Density-Tester ist das Hausner-Verhältnis. Dabei wird davon ausgegangen, dass stark kohäsive Pulver auch starke gegenseitige Anziehungskräfte besitzen. Diese helfen, die Schwerkraft zu überwinden, sodass die Partikel sich selbst in leeren Räumen stützen können
Reinigungsbewertung und Interpretation
Nach der Inkubation werden das Testgerät und das Referenzrohr auf das Vorhandensein von gelber Verfärbung des violetten MSHA untersucht. Es wird empfohlen, ein Raster mit einer 5x5 mm Skalierung und eine Farbabgleichsscheibe zu verwenden, um die Testergebnisse verschiedener Bediener zu standardisieren.
Die Scheibe enthält graduierte Farbtöne von Gelb bis Violett. Der Übergangspunkt, um als Gelb zu zählen, ist Farbton 3, Farbton 4 ist hellviolett. Ein kleiner gelber Bereich (ca. 5-30%) ist indikativ für eine normale Reinigungsverfahren des Referenzrohrs. Wenn der gelbe Bereich größer als 30% ist, sollte der Test wiederholt werden, da die Interpretation dieser Ergebnisse schwierig ist.
Im Allgemeinen sind drei Ergebnisse möglich, vorausgesetzt, es befindet sich eine kleine Menge Gelb im Referenzrohr:
- Vorhandensein von Milchresten,
- Vorhandensein von gelben Zonen und/oder Kolonien,
- Keine gelben Zonen/Kolonien.
Wenn beim Demontieren des Testobjekts sichtbare Milchreste festgestellt werden, bevor das Agar aufgebracht wurde, ist keine mikrobiologische Untersuchung erforderlich, da Sporen deutlich vorhanden sind. Es ist jedoch eine mikrobiologische Analyse des Referenzrohrs erforderlich, um zu bestätigen, dass die Reinigung akzeptabel war. Möglicherweise liegt ein hygienisches Designfehler des Testobjekts vor oder ein Fehler in der Testmethodologie. In diesem Fall muss der Test wiederholt werden. Wenn erneut Milchreste im gleichen Bereich gefunden werden, müssen vom Hersteller des Testobjekts Designänderungen vorgenommen werden. Handelte es sich um eine fehlerhafte Testmethode, muss dies behoben und der Test wiederholt werden.

Name: Juul Jenneskens
Berater
Nehmen Sie gerne Kontakt auf, wenn Sie Fragen zu diesem Thema haben. Gemeinsam mit meinen Kollegen stehe ich bereit, um Ihnen weiterzuhelfen!
Nehmen Sie Kontakt auf Juul Jenneskens 077 467 3555 [email protected]
Möchten Sie gerne direkt einen Kundenberater sprechen?
Testverfahren müssen maximal fünfmal wiederholt werden, um zu untersuchen, ob die gelben Zonen im Testobjekt zufällig verteilt sind oder auf ein schlechtes hygienisches Design hinweisen. Wenn in demselben Bereich des Testobjekts dreimal Schmutz zurückbleibt, deutet dies auf schwer zu reinigende Bereiche hin. Verbesserungen im hygienischen Design sollten in Betracht gezogen werden.
Wenn der Prozentsatz der gelben Zonen im Testobjekt mit dem des Referenzrohrs vergleichbar ist, ist auch der Grad der Reinigbarkeit vergleichbar. Ist der Prozentsatz der gelben Zonen im Testobjekt kleiner oder größer als im Referenzrohr, ist das Testobjekt mehr oder weniger gut reinigbar.
Es ist möglich, dass in einigen Fällen keine gelben Zonen im Testobjekt zurückbleiben. Wenn dies bei drei aufeinanderfolgenden Tests der Fall ist, sind keine weiteren Wiederholungen erforderlich, das Testobjekt kann als besonders gut reinigbar bezeichnet werden.
Gelegentlich liefern einige Dichtungsmaterialien falsch-negative Testergebnisse in Bereichen mit schlechtem hygienischen Design, während keine klaren gelben Zonen vorhanden sind. Dies kann daran liegen, dass das Dichtungsmaterial antibakterielle Eigenschaften besitzt, wodurch verhindert wird, dass Sporen, die auf seiner Oberfläche vorhanden sind, keimen und/oder wachsen.
Alle O-Ringe und Dichtungen im Testobjekt müssen auf antibakterielle Eigenschaften überprüft werden. Die Dichtung/O-Ringe können antibakterielle Eigenschaften aufweisen, wenn keine gelbe Verfärbung im Agar direkt um die Probe herum sichtbar wird. Der Test sollte mit Dichtungen/O-Ringen aus anderem Material durchgeführt werden, bis eine gelbe Verfärbung im Agar sichtbar wird.
Dichtungen/O-Ringe mit antibakteriellen Eigenschaften zeigen eine violette Zone um sich herum. Ein anderes Material muss verwendet werden, um den Test durchzuführen, bis keine violette Verfärbung mehr im gelben Agar beobachtet wird. Die Dichtungen/O-Ringe haben keine antibakteriellen Eigenschaften, wenn der Agar in den Petrischalen vollständig gelb ist.
