Karena meningkatnya kesadaran akan higiene pangan, European Hygienic Engineering and Design Group (EHEDG) didirikan.
Tujuan EHEDG adalah untuk meningkatkan keamanan produk dari sudut pandang ilmiah dan teknologi serta sesuai dengan peraturan EC mengenai desain higienis mesin makanan.
Artikel ini membahas:
- Pedoman desain higienis
- Prosedur pengujian
- Bagian pengujian prosedur pembersihan
- Deteksi residu tanah
- Penilaian dan interpretasi pembersihan
Para ahli Dinnissen Process Technology siap menjawab semua pertanyaan Anda:
Hubungi Juul Jenneskens 077 467 3555
Pedoman desain higienis
EHEDG telah menetapkan pedoman desain higienis yang dapat diverifikasi melalui prosedur uji standar terkait desain higienis. Pedoman ini mencakup aspek kemudahan pembersihan, kemampuan pasteurisasi, sterilisasi, dan aseptik.
Prosedur uji ini berfungsi sebagai tes penyaringan dasar untuk mengidentifikasi area dengan desain higienis yang kurang optimal serta area di mana produk atau mikroorganisme dapat terlindungi dari proses pembersihan. Selain itu, prosedur ini dapat digunakan untuk membandingkan peralatan berdasarkan kemudahan pembersihannya di tempat. Namun, tes ini tidak secara langsung mencerminkan kinerja dalam situasi pembersihan industri.
Tingkat kebersihan didasarkan pada penghilangan kotoran yang mengandung bakteri dan dinilai dengan mengevaluasi pertumbuhan bakteri residu setelah pembersihan. Istilah berikut digunakan dalam konteks ini:
- Pembersihan: penghilangan kotoran, sisa makanan, debu, minyak, atau zat pengganggu lainnya,
- Kemudahan pembersihan: kesesuaian peralatan untuk dibersihkan dengan mudah dari kotoran,
- Kemudahan pembersihan komparatif: kemudahan pembersihan suatu peralatan dibandingkan dengan referensi,
- Kemudahan pembersihan di tempat: kemampuan peralatan untuk dibersihkan dengan mudah tanpa perlu dibongkar.

EHEDG
Prosedur uji
Pertama, bagian uji harus dibentuk. Ini dilakukan dengan menghubungkan peralatan yang akan diuji ke pipa referensi sepanjang 250 mm. Pipa ini memiliki tingkat kekasaran permukaan internal yang diketahui (rata-rata Ra = 0,5 - 0,7 mikron atau setara menurut ISO 4287:1977) dan dua segmen pendek tambahan yang dipasang di kedua ujungnya untuk membentuk bagian uji.
Setelah itu, bagian uji diisi dengan susu asam dan kedua ujungnya ditutup. Selanjutnya, bagian ini diberi tekanan tiga kali hingga 5 bar menggunakan pelat penutup dengan sambungan udara yang sesuai, selama dua menit. Dalam tahap ini, semua bagian yang dapat bergerak dioperasikan untuk mensimulasikan kondisi kerja dari bagian uji. Sebanyak 10 operasi harus dilakukan dalam tiga periode pemberian tekanan ini.
Kemudian, susu asam dikosongkan dan bagian uji dikeringkan dengan dibilas menggunakan udara kering yang telah difilter.
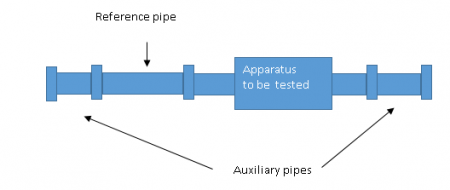
Prosedur pengujian
Prosedur pembersihan bagian uji
Untuk proses pembersihan, area uji yang kotor dipasang dalam sistem uji khusus tanpa melepas pipa tambahan. Sebuah tabung lurus, dengan panjang setidaknya lima kali diameter pipa referensi, harus dipasang sebelum dan sesudah bagian uji untuk memastikan aliran larutan pembersih yang stabil melalui bagian uji. Setelah itu, prosedur pembersihan berikut dapat dimulai:
- Bilas dengan air dingin (10-200°C) selama waktu yang setara dengan waktu tinggal rata-rata (t) dan tidak kurang dari 1 menit,
- Sirkulasikan larutan deterjen 1% (w/v) pada suhu 630°C ± 20°C selama 10 menit (volume larutan deterjen yang digunakan harus setidaknya 20 kali volume internal bagian uji),
- Bilas dengan air dingin (10-200°C) selama waktu yang setara dengan waktu tinggal rata-rata (t) dan tidak kurang dari 1 menit.
- Di mana waktu tinggal rata-rata (t) = volume bagian uji / laju aliran.
Pada outlet peralatan, sampel air diambil seakurat mungkin dari kedua kali pembilasan setelah prosedur pembilasan selesai. Dua sampel masing-masing 5 ml dituangkan dengan MSHA ke dalam cawan petri. Pembilasan awal harus dapat memulihkan 3-300 spora per 10 ml. Setelah pembilasan akhir, kurang dari 1 spora per 10 ml harus ditemukan. Jika dalam pembilasan awal ditemukan kurang dari 1 spora per 10 ml atau jika spora masih ada dalam pembilasan akhir, ini dapat mengindikasikan prosedur uji yang tidak memadai dan dapat menyebabkan hasil yang salah.
Deteksi residu tanah
Setelah proses pembersihan selesai, bagian uji dikeluarkan dari sistem uji. Permukaan bagian dalam pipa referensi kemudian dilapisi dengan MSHA cair hingga ketebalan setidaknya 5 mm, mencakup semua permukaan relevan dari peralatan uji. Setelah agar sepenuhnya mengeras, pipa referensi ditempatkan dalam posisi hampir vertikal di inkubator dengan suhu 58°C selama 24 jam. Kondensasi dalam pipa referensi dapat menyebarkan mikroorganisme dan/atau produk metabolik mikroba yang bersifat asam sepanjang pipa referensi selama proses inkubasi. Dalam kondisi ini, hasil pembacaan yang salah dapat terjadi, ditandai dengan perubahan warna menjadi kuning.
Prosedur uji ini merupakan tes penyaringan dasar untuk mengidentifikasi area dengan desain higienis yang kurang baik serta tempat di mana produk atau mikroorganisme terlindung dari proses pembersihan.
Penilaian dan interpretasi pembersihan
Setelah inkubasi, peralatan uji dan pipa referensi diperiksa untuk melihat adanya perubahan warna kuning pada MSHA ungu. Disarankan untuk menggunakan skala grid 5x5 mm dan cakram perbandingan warna guna menstandarisasi hasil uji dari berbagai operator.
Cakram tersebut berisi gradasi warna dari kuning hingga ungu. Titik transisi untuk dianggap sebagai kuning adalah tingkat warna 3, sedangkan tingkat warna 4 adalah ungu muda. Sebagai indikasi prosedur pembersihan pipa referensi yang normal, area kuning yang kecil (sekitar 5-30%) masih dapat diterima. Jika area kuning lebih besar dari 30%, uji harus diulang karena interpretasi hasil menjadi sulit.
Secara umum, tiga hasil yang mungkin terjadi, dengan asumsi terdapat sedikit warna kuning dalam pipa referensi:
- Kehadiran residu susu,
- Kehadiran zona kuning dan/atau koloni,
- Tidak ada zona kuning/koloni.
Jika residu susu terlihat sebelum agar diterapkan saat membongkar objek uji, maka pemeriksaan mikrobiologis tidak diperlukan karena jejak kontaminasi sudah jelas ada. Namun, analisis mikrobiologis pada pipa referensi tetap diperlukan untuk memastikan bahwa pembersihan telah dilakukan dengan baik. Jika ditemukan kekurangan dalam desain higienis pada objek uji atau kesalahan dalam metode pengujian, uji harus diulang. Jika residu susu ditemukan kembali di area yang sama, perubahan desain harus dilakukan oleh produsen objek uji. Jika metode uji terbukti salah, metode tersebut harus diperbaiki dan uji diulang.
Prosedur pengujian harus diulang hingga lima kali untuk menentukan apakah zona kuning pada objek uji tersebar secara acak atau menunjukkan desain higienis yang kurang baik. Jika sisa kontaminasi ditemukan di area yang sama sebanyak tiga kali dalam spesimen uji, ini menunjukkan area yang sulit dibersihkan. Dalam hal ini, perlu dipertimbangkan perbaikan dalam desain higienis.
Jika persentase zona kuning pada objek uji sebanding dengan yang ada pada pipa referensi, maka tingkat kemudahan pembersihannya juga dianggap setara. Jika persentase zona kuning pada objek uji lebih kecil atau lebih besar dari pipa referensi, maka objek uji lebih atau kurang dapat dibersihkan.
Dalam beberapa kasus, mungkin tidak ada zona kuning yang tersisa dalam objek uji. Jika hal ini terjadi dalam tiga kali pengujian berturut-turut, maka tidak diperlukan uji tambahan lebih lanjut dan objek uji dapat dianggap sangat mudah dibersihkan. Kadang-kadang, beberapa bahan gasket dapat memberikan hasil uji negatif palsu di area dengan desain higienis yang buruk, meskipun tidak ada zona kuning yang terlihat. Hal ini dapat terjadi karena bahan kemasan memiliki sifat antibakteri, yang mencegah spora pada permukaannya berkecambah dan/atau berkembang biak.
Semua o-ring dan gasket dalam objek uji harus diperiksa apakah memiliki sifat antibakteri. Gasket atau o-ring dapat memiliki sifat antibakteri jika tidak ada perubahan warna kuning yang terlihat pada agar di sekitar sampel. Uji harus dilakukan dengan gasket atau o-ring dari bahan lain hingga perubahan warna kuning terlihat pada agar. Gasket atau o-ring dengan sifat antibakteri akan menunjukkan zona ungu di sekitarnya. Pengujian harus dilakukan dengan bahan lain hingga tidak ada perubahan warna ungu dalam agar kuning. Gasket atau o-ring tidak memiliki sifat antibakteri jika agar dalam cawan petri sepenuhnya berwarna kuning.

Nama: Juul Jenneskens
Penasihat
Jangan ragu untuk menghubungi kami jika Anda memiliki pertanyaan mengenai topik ini. Saya dan rekan-rekan saya siap membantu Anda!
Hubungi Juul Jenneskens 077 467 3555 [email protected]
Apakah Anda ingin meminta konsultasi langsung?
