Vanwege het toegenomen bewustzijn rond voedselhygiëne is de European Hygienic Engineering and Design Group (EHEDG) opgericht.
Dit artikel zal ingaan op:
- Hygiënische ontwerplijnen
- Testprocedure
- Testgedeelte reinigingsprocedure
- Detectie van restaarde
- Reinigingsbeoordeling en interpretatie
De experts van Dinnissen Process Technology staan klaar voor al uw vragen:
Neem contact op met Juul Jenneskens 077 467 3555
Hygiënische ontwerplijnen
EHEDG heeft hygiënische ontwerprichtlijnen opgesteld die kunnen worden geverifieerd door standaardtestprocedures, gerelateerd aan hygiënisch ontwerp. Dit is inclusief reinigbaarheid, pasteuriseerbaarheid, serialiseerbaarheid en aseptisch vermogen.
De testprocedure is een basale screeningtest om gebieden met een slecht hygiënisch ontwerp en waar product- of micro-organismen worden beschermd tegen de werking van het reinigingsproces te identificeren. Het kan ook worden gebruikt om apparaten te vergelijken met betrekking tot hun reinigbaarheid op hun plaats. De test is niet indicatief voor prestaties in industriële reinigingssituaties.
De reinheidsgraad is gebaseerd op het verwijderen van een bodem die bacteriën bevat en wordt beoordeeld door de groei van achtergebleven bacteriën na het reinigen te evalueren. De volgende begrippen worden hiervoor gebruikt:
- Reiniging: het verwijderen van grond, voedselresten, vuil, vet of andere hinderlijke stoffen,
- Reinigbaarheid: de geschiktheid van apparatuur om gemakkelijk van grond te worden bevrijd,
- Vergelijkende reinigbaarheid: de reinigbaarheid van apparatuur ten opzichte van een referentie,
- Reinigbaarheid ter plaatse: de geschiktheid om gemakkelijk te worden gereinigd zonder demontage.

EHEDG
Testprocedure
Ten eerste moet er een testsectie worden gevormd. Dit wordt gedaan door de te testen apparatuur te koppelen aan een referentiepijp van 250 mm. Met de bekende interne oppervlakteruwheid (gemiddeld Ra = 0,5 - 0,7 micron of equivalent volgens ISO 4287: 1977) en met twee korte hulplengtes gemaakt van buis aan elk uiteinde om een testsectie te vormen.
Hierna wordt het testgedeelte gevuld met zure melk en worden beide uiteinden gesloten. Hierna wordt het drie keer onder druk gebracht tot 5 bar, met behulp van een afsluitplaat met een geschikte luchtkoppeling, gedurende twee minuten. Het is mogelijk om een ingebruikname situatie van de testsectie te stimuleren door alle beweegbare onderdelen te bedienen. Er moeten in totaal 10 operaties worden uitgevoerd binnen de 3 onder druk gezette perioden.
Vervolgens wordt de zure melk afgegoten en het testgedeelte gedroogd door te spoelen met droge gefilterde lucht.
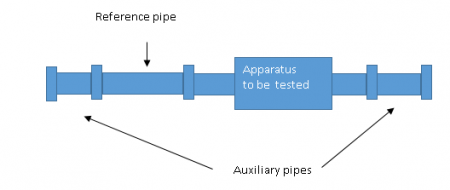
Testprocedure
Testgedeelte reinigingsprocedure
Voor het reinigen wordt het vuile testgedeelte gemonteerd in een speciaal daarvoor gebouwde testopstelling, zonder de hulpleidingen te verwijderen. Een rechte buis met een lengte van minstens vijf keer de diameter van de referentiepijp, moet voor en na het testgedeelte worden ingebracht om een gestabiliseerde stroom reinigingsoplossing door het testgedeelte te garanderen. Dan kan de volgende reinigingsprocedure beginnen:
- Spoel met koud water (10-200C) gedurende een tijd die gelijk is aan de gemiddelde verblijftijd (t) en niet minder dan 1 minuut,
- Circuleer een 1% (w / v) wasmiddeloplossing bij 630C +/- 20C gedurende 10 minuten (het volume van de gebruikte wasmiddeloplossing moet minstens 20 keer het interne volume van het testitem zijn),
- Spoel met koud water (10-200C) gedurende een tijd die gelijk is aan de gemiddelde verblijftijd (t) en niet minder dan 1 minuut.
Waar gemiddelde verblijftijd (t) = volume van testitem / stroomsnelheid.
Aan de uitlaat van de apparatuur worden aan het einde van de spoelprocedures zo nauwkeurig mogelijk watermonsters genomen van beide spoelbeurten. Per petrischaal worden twee monsters van 5 ml gegoten met MSHA. Bij het voorspoelen zullen er 3-300 sporen per 10 ml worden teruggewonnen. Na de laatste spoeling moet <1 sporen per 10 ml worden hersteld. Minder dan 1 sporen per 10 ml in de voorspoeling of de aanwezigheid van sporen in de laatste spoeling, kan wijzen op een onvoldoende testprocedure en zou tot valse resultaten kunnen leiden.
Detectie van restaarde
Na het reinigen wordt het testgedeelte van de rig verwijderd. Het binnen oppervlak van de referentiepijp is bedekt met gesmolten MSHA tot een dikte van ten minste 5 mm, inclusief alle relevante oppervlakken van de testapparatuur. Nadat de agar volledig is gestold, wordt de referentiepijp gedurende 24 uur bijna verticaal in een incubator van 580 geplaatst. Het is mogelijk dat condensatie in de referentiepijp tijdens incubatie micro-organismen en / of zure microbiële metabole producten langs de referentiepijp verspreidt. In deze situatie wordt een verkeerde aflezing van gele verkleuring verkregen.
De testprocedure is een basale screeningtest om gebieden met een slecht hygiënisch ontwerp te identificeren en waar product- of micro-organismen worden beschermd tegen de werking van het reinigingsproces
Reinigingsbeoordeling en interpretatie
Na incubatie worden de testapparatuur en referentiepijp onderzocht op de aanwezigheid van gele verkleuring van de paarse MSHA. Het wordt aangeraden een raster met 5x5 mm-schaalverdeling en een kleurvergelijkingsschijf te gebruiken om de testresultaten van verschillende operators te standaardiseren.
De schijf bevat gegradueerde tinten geel tot paars. Het overgangspunt om als geel te tellen is tint 3, tint 4 is lichtpaars. Indicatief voor een normale reinigingsprocedure van de referentiepijp is een klein geel gebied (ca. 5-30%). Als het gele gebied groter is dan 30%, moet de test worden herhaald, omdat interpretatie van deze resultaten moeilijk is.
Over het algemeen zijn drie resultaten mogelijk, ervan uitgaande dat er een kleine hoeveelheid geel in de referentiepijp zit:
- Aanwezigheid van melkresten,
- Aanwezigheid van gele zones en / of kolonies,
- Geen gele zones / kolonies.
Als er bij het demonteren van het testobject zichtbare melkresten worden waargenomen voordat de agar is aangebracht, is er geen microbiologisch onderzoek nodig aangezien sporen duidelijk aanwezig zijn. Er is echter een microbiologische analyse van de referentiepijp vereist om te bevestigen dat de reiniging acceptabel was. Er kan een hygiënische ontwerpfout zijn die inherent is aan het testitem of een fout in de testmethodologie. Hierna moet de test worden herhaald. Als er weer melkresten worden gevonden in hetzelfde gebied, moeten ontwerpwijzigingen worden aangebracht door de fabrikant van het testitem. Als het om een foutieve testmethode ging, moet dit worden verholpen en moet de test worden herhaald.

Naam: Juul Jenneskens
Adviseur
Neem gerust contact op als u vragen heeft over dit onderwerp. Samen met mijn collega's sta ik klaar om u te helpen!
Neem contact op met Juul Jenneskens 077 467 3555 [email protected]
Liever direct een adviesgesprek aanvragen?
Testprocedures moeten maximaal vijf keer worden herhaald, om te onderzoeken of gele zones in het testitem willekeurig zijn verdeeld of duiden op een slecht hygiënisch ontwerp. Als er in hetzelfde gebied van het testitem drie keer grond is achtergebleven, duidt dit op gebieden die moeilijk schoon te maken zijn. Verbeteringen in het hygiënisch ontwerp moeten worden overwogen.
Als het percentage gele zones in het testitem vergelijkbaar is met dat van de referentiepijp, dan is ook de mate van reinigbaarheid vergelijkbaar. Is het percentage gele zones in het testitem kleiner of groter dan de referentiepijp, dan is het testitem min of meer reinigbaar.
Het is mogelijk dat er in sommige gevallen geen gele zones achterblijven in het testitem. Als dit bij drie opeenvolgende gelegenheden is, zijn er geen verdere testherhalingen nodig, het testitem kan worden omschreven als bijzonder reinigbaar.
Af en toe geven sommige pakkingmaterialen vals-negatieve testresultaten bij gebieden met een slecht hygiënisch ontwerp, terwijl er geen duidelijke gele zones zijn. Dit kan doordat het pakkingmateriaal antibacteriële eigenschappen heeft, zodat wordt voorkomen dat sporen die op hun oppervlak aanwezig zijn, ontkiemen en / of groeien.
Alle o-ringen en pakkingen in het testitem moeten worden gecontroleerd op antibacteriële eigenschappen. De pakking / o-ringen kunnen antibacteriële eigenschappen hebben als er geen gele verkleuring zichtbaar wordt in de agar, direct rond het monster. De test moet worden uitgevoerd met pakkingen / o-ringen van een ander materiaal totdat gele verkleuring zichtbaar wordt in de agar.
Pakkingen / o-ring met antibacteriële eigenschappen vertonen een paarse zone om hen heen. Er moet een ander materiaal worden gebruikt om de test uit te voeren totdat er geen paarse verkleuring wordt waargenomen in de gele agar. De pakkingen / o-ringen hebben geen antibacteriële eigenschappen als de agar in de petrischalen helemaal geel is.
